Chỉnh sửa biểu sinh dựa trên CRISPR: Xu hướng mới trong điều hòa biểu hiện gene
Công nghệ chỉnh sửa gene CRISPR-Cas9 ngày càng phát triển mạnh mẽ và được ứng dụng rộng rãi trong nhiều nghiên cứu cơ bản và điều trị bệnh. Trong những năm gần đây, bên cạnh chức năng chỉnh sửa gene, các công nghệ dựa trên CRISPR còn được khai thác để điều hòa biểu hiện gene thông qua biến đổi biểu sinh mà không làm đứt gãy DNA (Hình 1). Hướng tiếp cận này có độ an toàn cao hơn so với phương pháp truyền thống và có tiềm năng ứng dụng trong lĩnh vực y sinh.
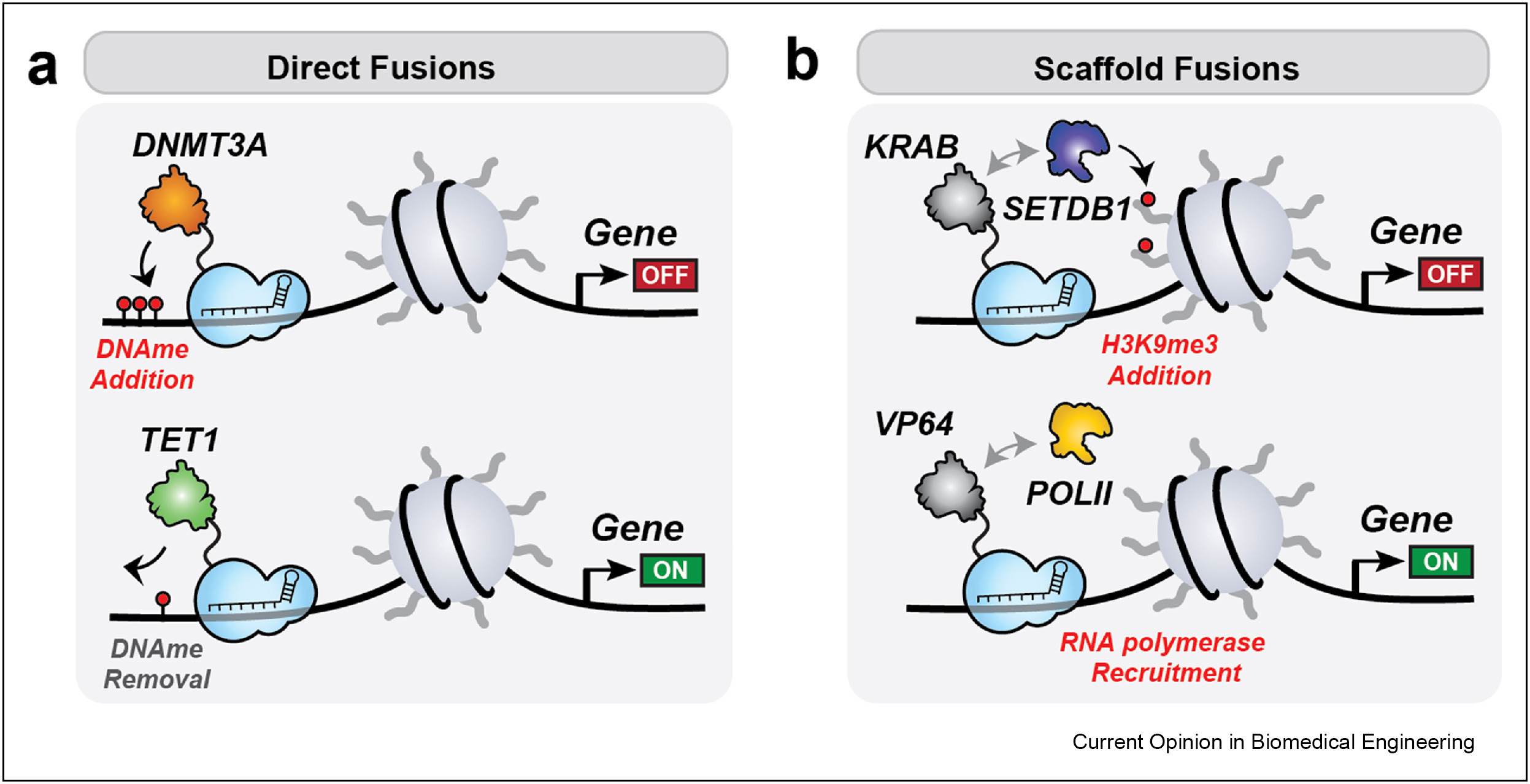
Hình 1. Công nghệ CRISPR điều hòa biểu sinh và phiên mã mà không cắt DNA. Hình minh họa 2 chiến lược chính: (a) dCas9 gắn trực tiếp với enzyme biến đổi biểu sinh, cho phép tác động tại vị trí mục tiêu trên DNA hoặc chromatin. Ví dụ, DNMT3A xúc tác gắn thêm nhóm methyl vào DNA làm im lặng gene hoặc TET1 loại bỏ các nhóm methyl để hoạt hóa gene mục tiêu; (b) dCas9 gắn kết với các protein trung gian, các protein này sẽ thu hút các yếu tố nội sinh trong tế bào để điều hòa biểu hiện gene. Ví dụ, KRAB giúp gắn thu hút protein ức chế SETDB1 gây im lặng gene hoặc VP64/VPR thu hút RNA polymerase II giúp kích hoạt phiên mã gene mục tiêu.
Hệ thống chỉnh sửa biểu sinh có 2 thành phần chính bao gồm protein gắn DNA (dCas9) và effector biểu sinh. Cơ chế hoạt động dựa trên việc sử dụng protein Cas9 đã bị ức chế khả năng cắt DNA (dCas9), chỉ giữ lại khả năng nhận diện và gắn kết với DNA mục tiêu. Từ đó, thông qua các effector tương ứng, trạng thái chromatin thay đổi sang dạng hoạt hóa hay bất hoạt. Hệ thống chỉnh sửa biểu sinh có 2 dạng là CRISPRi và CRISPRa với vai trò tương ứng là ức chế hoặc hoạt hóa gene mục tiêu. Nhờ ưu điểm của việc không gây đứt gãy DNA và có thể điều chỉnh linh hoạt biểu hiện gene, công nghệ này được ứng dụng rộng rãi trong nghiên cứu chức năng gene và thiết lập mô hình bệnh.
Trước đây, việc tìm kiếm các effector mới thường tốn nhiều thời gian và cần tối ưu nhiều lần. Gần đây, sự phát triển của các hệ thống sàng lọc thông lượng cao (high-throughput) đã giúp phát hiện hàng nghìn effector mới với hoạt tính tối ưu hơn. Đồng thời, các hệ activator/repressor mới cũng được phát triển với ưu điểm nhỏ gọn và ít gây miễn dịch như CRISPR-DREAM và NFZ. Bên cạnh đó, các chiến lược kết hợp nhiều effector đã tăng hiệu quả điều hòa biểu hiện gene lâu dài. Từ đó, các hướng chiến lược này giúp mô phỏng tốt hơn cơ chế điều hòa gene tự nhiên trong tế bào.
Công nghệ chỉnh sửa biểu sinh mang tiềm năng lớn trong điều trị bệnh, đặc biệt trong y học cá thể và liệu pháp gene. Một số ứng dụng điển hình có thể nhắc đến thông qua hệ thống CRISPRi bao gồm: ức chế gene MGMT làm tăng hiệu quả hóa trị ung thư; ức chế Pcsk9 giúp giảm cholesterol; ức chế DNA virus HBV, hướng tới điều trị lâu dài. Bên cạnh đó, hệ thống CRISPRa hỗ trợ trong việc tăng biểu hiện các gene thiếu hụt, ví dụ như việc phục hồi chức năng gene Scn2a giúp cải thiện chức năng neuron trong rối loạn thần kinh, giảm nguy cơ co giật ở chuột.
Tuy nhiên, công nghệ này vẫn đối diện những thách thức lớn trong nghiên cứu và ứng dụng lâm sàng. Đầu tiên, các tác động ngoài ý muốn (off-target) có thể gây biến đổi biểu hiện gene không mong muốn kéo dài và ảnh hưởng rộng, đặc biệt khi xảy ra ở promoter hoặc enhancer. Bên cạnh đó, hệ thống chỉnh sửa biểu sinh thường có kích thước lớn, gây khó khăn trong việc vận chuyển vào tế bào. Hiệu quả chỉnh sửa phụ thuộc nhiều vào loại tế bào, chromatin và trình tự DNA, gây khó khăn trong việc so sánh giữa các nghiên cứu. Vì vậy, hệ thống này cần đảm bảo an toàn và hiệu quả trước khi ứng dụng lâm sàng. Một số hướng khắc phục đã được triển khai và mang lại hiệu quả như thiết kế hệ thống nhỏ gọn, an toàn; hiểu rõ cơ chế biểu sinh và phiên mã; giảm off-target và tăng độ chính xác; so sánh và chuẩn hóa các công cụ.
Nhìn chung, công nghệ chỉnh sửa biểu sinh đang phát triển rất nhanh, đặc biệt với sự tiến bộ của công nghệ sàng lọc thông lượng cao, giúp phát hiện nhiều effector mới. Đến nay, nhiều nghiên cứu trên mô hình động vật đã có kết quả khả quan và tiến gần tới thử nghiệm lâm sàng. Tuy nhiên, để tối ưu hóa hiệu quả sử dụng, các nhà khoa học cần hiểu rõ hơn về cơ chế hoạt động của effector, đánh giá off-target và độc tính. Việc giải quyết các thách thức này giúp nâng cao độ an toàn và hiệu quả, mở rộng ứng dụng trong nghiên cứu và y học chính xác.
Tài liệu tham khảo
Pattali, R. K., Divekar, N. S., & Nuñez, J. K. (2026). Next generation technologies for CRISPR-based epigenome and transcriptional modulation. Current Opinion in Biomedical Engineering, 100654. https://doi.org/10.1016/j.cobme.2026.100654
Người đăng bài: ThS. Phan Thủy Quyên

